a cuea di Andrea Ricotti, Andrea Pierini, Francesca Pietribiasi, Gianfranco Cassissa, Danilo Bono, Giovanni Messori Ioli, Fulvio Moirano, Renato Botti, Oscar Bertetto,
1. ASL CN2
2. Dipartimento Funzionale Interaziendale Interregionale Rete Oncologica Del Piemonte e Della Valle D’Aosta
3. Direttore Generale dell’Assessorato alla Sanità Piemontese
4. ATS Sardegna
5. Market Access, Roche S.p.A
6. Direttore Anatomia Patologica ASL TO5
1. Introduzione
La sostenibilità del sistema sanitario italiano è minata da diversi fattori. L’aumento della domanda di servizi e prestazioni da parte di cittadini e pazienti, il progressivo invecchiamento della popolazione, il costo crescente delle innovazioni, con particolare riferimento a quelle farmacologiche, sono gli elementi di maggiore impatto socio-economico [1]. A tal fine il recente DPCM del 12 gennaio 2017 pone le premesse per ridefinire i nuovi Livelli Essenziali di Assistenza (LEA), tenendo in considerazione anche le evidenze di efficacia ed il concetto di value, definito come il ritorno in termini di salute delle risorse investite in sanità (rapporto tra outcome e costi), pur senza esplicitare la metodologia da utilizzare per la loro definizione. Come riportato nel “2° Rapporto GIMBE – 2017”: “il problema della sostenibilità non è di natura squisitamente finanziaria, perché un’aumentata disponibilità di risorse non permette di risolvere cinque tra le maggiori criticità ampiamente documentate nei paesi industrializzati: l’estrema variabilità nell’utilizzo di servizi e prestazioni sanitarie; gli effetti avversi dell’eccesso di medicalizzazione; le diseguaglianze conseguenti al sottoutilizzo di servizi e prestazioni sanitarie dall’elevato value; l’incapacità di attuare efficaci strategie di prevenzione; gli sprechi, che si annidano a tutti i livelli”. Sicuramente “governare” l’estrema complessità delle organizzazioni sanitarie avendo come duplice obiettivo sia la promozione dell’efficacia/qualità assistenziale che dell’efficienza, in relazione alla sostenibilità economica, non è attuabile in modo scontato. Inoltre, si deve aggiungere il gap esistente tra professionisti (libertà professionale incondizionata) e manager (bilancio aziendale) [2]. Probabilmente alcuni miglioramenti si potrebbero registrare passando da una Governance basata sui budget a “silos” e quindi a singole variabili per lasciare strada ad una gestione che tenga conto dell’intero percorso diagnostico terapeutico ed assistenziale (PDTA) e quindi ad un approccio multidimensionale. Si tratterebbe di un passaggio chiave perché, finalmente, porrebbe il paziente al centro del suo percorso di malattia. A tal fine, sarebbe opportuno mettere a punto un sistema specifico di indicatori per monitorare la qualità dell’assistenza sanitaria, in termini di sicurezza, efficacia, appropriatezza, partecipazione degli utenti, equità, efficienza [2]. Si potrebbe pertanto finalmente attuare un piano di disinvestimento da sprechi e inefficienze, basato non solo su azioni puntuali di spending review, ma che preveda interventi strutturali e organizzativi di riallocazione di risorse [1]. A tal proposito la Clinical Governance (CG) fornisce, attraverso alcune delle sue aree (Evidence Based Medicine, Information & Data Management, Linee Guida e PDTA, Audit clinici), strumenti operativi utili per declinare azioni concrete mediante le quali le organizzazioni sanitarie si rendono responsabili del miglioramento continuo della qualità dei servizi e del raggiungimento/mantenimento di elevati standard assistenziali, stimolando la creazione di un ambiente che favorisca l’eccellenza professionale [2]. Si è proceduto in tale direzione andando ad esplorare un percorso di cura in ambito oncologico, mediante lo studio di seguito riportato, condotto con il supporto scientifico della Rete Oncologica Piemonte/Valle d’Aosta e basato sulle aree della CG sopra evidenziate, utilizzando la metodologia E.Pic.A. (Appropriatezza Economica del Percorso integrato di cura) proposta da Massa et al. [3],. L’approccio metodologico del progetto si è basato sullo sviluppo di un modello di analisi, che a partire dal percorso post-diagnosi della paziente con tumore della mammella, è stato alimentato da dati di Real World Evidence (RWE), estrapolati da database amministrativi e clinici delle aziende sanitarie locali. L’analisi è stata condotta basandosi su un set di indicatori (Key Performance Indicators – KPI), selezionati da un panel di esperti sulla base di evidenze di letteratura.
2. Metodi
2.1 Coorte
Lo studio è stato condotto su un gruppo di pazienti affette da tumore maligno della mammella
afferite alle strutture piemontesi dal 1 gennaio al 31 dicembre 2015.
2.2 Key Performance Indicators
È stato eseguito un nuovo approccio di valutazione delle performance come proposto dallo studio E.Pic.A., basandosi su l’identificazione di 7 Key Performance Indicators (KPI) scelti da un gruppo di professionisti esperti selezionato dalla Rete Oncologica Piemontese partendo dalle linee guida dell’Associazione Italiana di Oncologia Medica (AIOM) [5]. Lo scopo è stato quello di analizzare il percorso di cura diagnostico e terapeutico delle donne affette da tumore della mammella per ciò che concerne la diagnostica, gli interventi eseguiti in chirurgia e gli interventi di radio e chemioterapia. I KPI sono stati così definiti: KPI 1, proporzione di pazienti in stadio 0, I o II di malattia che hanno eseguito nei due mesi precedenti l’intervento chirurgico uno tra i seguenti accertamenti: ecografia (ECO) epatica, Tomografia Computerizzata (TAC), Risonanza Magnetica Nucleare (RMN) eccetto torace o mammella, scintigrafia ossea o Positron Emission Tomography (PET); KPI 2, proporzione di pazienti in stadio 0, I o II di malattia che hanno eseguito nei due mesi successivi l’intervento chirurgico uno tra i seguenti accertamenti: ECO epatica, TAC, RMN (eccetto torace o mammella), scintigrafia ossea o PET; KPI 3, proporzione di pazienti che è stata sottosposta a svuotamento ascellare e/o ricostruzione nei 3 mesi successivi l’intervento chirurgico di mastectomia; KPI 4, proporzione di pazienti che è stata sottosposta a re-intervento chirurgico con il calcolo del tempo medio di re-intervento; KPI 5, proporzione di pazienti che ha iniziato la terapia adiuvante entro 60 giorni dall’intervento chirurgico; KPI 6, proporzione di pazienti che ha eseguito la radioterapia entro 90 o 150 giorni dall’ultimo intervento chirurgico se non erano candidate a trattamento adiuvante, oppure entro 180 o 270 giorni dall’ultimo intervento chirurgico se erano candidate a trattamento adiuvante; KPI 7, proporzione di pazienti in stadio 0, I o II di malattia che hanno eseguito nei dodici mesi successivi l’intervento chirurgico uno tra i seguenti accertamenti: ECO epatica, TAC, RMN (eccetto torace e mammella), scintigrafia ossea o PET; escludendo i primi due mesi analizzati nel KPI 2.
2.3 Analisi Dati
La coorte è stata selezionata basandosi sui codici ICD-9-CM di diagnosi principale o secondaria di tumore maligno della mammella (ICD-9-CM 174.x e 233.0) ed intervento chirurgico principale o secondario di quadrantectomia o mastectomia (ICD-9-CM 85.33, 85.34, 85.35, 85.36, 85.2x o 85.4x) [4]. I dati per il calcolo dei KPI sono stati estratti andando ad eseguire un cross-linkage tra i flussi: • Ricoveri ospedalieri • Prestazioni ambulatoriali • DPC (Distribuzione Per Conto) • Farmaceutica convenzionata La stadiazione del carcinoma mammario è stata definita mediante l’utilizzo della classificazione TNM (Tumor, Node, Metastasis) riportata dal referto di anatomia patologica presente sulla banca dati della Scheda computerizzata per il controllo della Qualità del Trattamento del carcinoma Mammario (SQTM). È stato definito come indicatore proxy di tumore primario il non aver subito un intervento nei 365 giorni precedenti all’intervento eseguito nel 2015.
3. Risultati
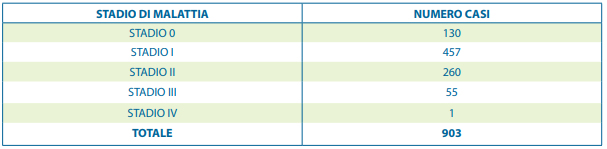
È stata selezionata una coorte di 903 pazienti di sesso femminile così ripartiti in base allo
stadiazione TNM:
Tabella 1 – Pazienti suddivisi per stadio di malattia
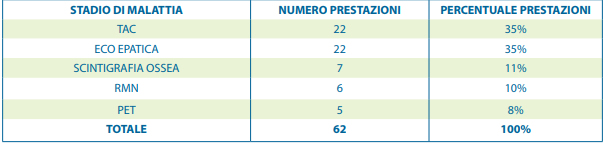
KPI 1 – Dall’analisi dei dati estratti dei flussi informativi ne è emerso che 43 (5%) delle 847 pazienti in stadio 0, I o II di malattia sono state sottoposte nei due mesi precedenti l’intervento chirurgico a uno tra i seguenti accertamenti: ECO epatica, TAC, RMN (eccetto torace o mammella), scintigrafia ossea o PET. Le diagnostiche totali eseguite sono state 62 con una media di circa 1.44 prestazioni per paziente.
Tabella 2 – Elenco prestazioni inappropriate nei due mesi precedenti l’intervento chirurgico
KPI 2 – Nei 2 mesi successivi l’intervento chirurgico, 307 (36%) delle 847 pazienti in stadio 0, I o II di malattia sono state sottoposte nei due mesi successivi l’intervento chirurgico a uno tra i seguenti accertamenti: ECO epatica, TAC, RMN (eccetto torace o mammella), scintigrafia ossea o PET. Le diagnostiche totali eseguite sono state 505 con una media di circa 1.64 prestazioni per paziente.
Tabella 3 – Elenco prestazioni inappropriate nei due mesi successivi l’intervento chirurgico
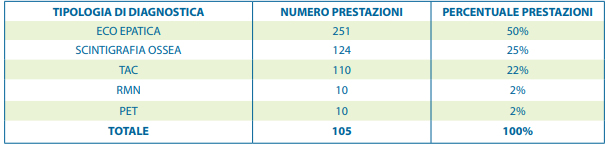
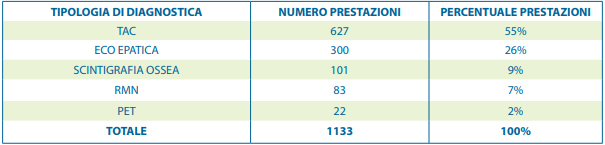
KPI 3 – Per ciò che concerne la fase chirurgica, 12 (9%) delle 136 pazienti sottoposte a mastectomia come primo intervento, hanno eseguito uno svuotamento ascellare nei 3 mesi successivi l’intervento chirurgico. Nessuna delle suddette è stata sottoposta ad un ricostruzione della mammella nei 3 mesi successivi alla mastectomia come primo intervento. KPI 4 – Delle 903 pazienti operate di carcinoma della mammella, 34 (4%) sono state sottoposte a re-intervento chirurgico con un tempo medio pari a 54 giorni. KPI 5 – Per ciò che concerne la terapia adiuvante, 549 (71%) su 769 pazienti hanno iniziato la terapia farmacologica entro 60 giorni dall’ultimo intervento chirurgico. KPI 6 – Le procedure radioterapiche sono state eseguite entro 90 giorni, dall’ultimo intervento chirurgico, su 19 (23%) pazienti a fronte delle 83 non sottoposte a terapia adiu-vante; il numero di pazienti sale a 53 (70%) entro 150 giorni. Il numero di donne sottoposte a terapia adiuvante a cui è stata associata una procedura radioterapica entro 180 giorni dall’ultimo intervento chirurgico sono state 425 (73%) su 581, la quota di trattate sale fino a 549 (94%) considerando 270 giorni. KPI 7 – Durante la fase di follow-up, 611 (72%) delle 847 pazienti in stadio 0, I o II di malattia sono state sottoposte nei dodici mesi successivi l’intervento chirurgico (escludendo i primi due mesi analizzati nel KPI 2) ad uno tra i seguenti accertamenti: ECO epatica, TAC, RMN (eccetto torace o mammella), scintigrafia ossea o PET. Le diagnostiche totali eseguite sono state 1133 con una media di circa 1.85 prestazioni per paziente.
Tabella 4 – Elenco prestazioni inappropriate eseguite durante il follow-up
Discussione
L’analisi effettuata mediante cross-linkage dei database ha evidenziato interessanti risultati utili per un possibile processo di Governance sia a livello aziendale che di sistema, pur nella consapevolezza della presenza di un bias di compilazioni nei flussi informativi. Durante la fase di diagnostica, è stato riscontrato un sovra-utilizzo delle metodiche anche se in misura limitata durante i due mesi che precedono l’intervento (KPI 1) in misura pari al 5%; per ciò che concerne la fase post-intervento (KPI 2), invece, si evidenzia una percentuale del 36% di pazienti con prestazioni non appropriate eseguite (over-use), in una proporzione tale da risultare idoneo un approfondimento attraverso Audit clinici. L’analisi inerente l’attività chirurgica ha evidenziato con il KPI 3 che una quota di pazienti (9%) è stata sottoposta allo svuotamento dei linfonodi ascellari entro tre mesi dall’intervento di mastectomia. Tale fenomeno può essere riconducibile all’assenza in alcune realtà aziendali della diagnostica in sede operatoria finalizzata al riconoscimento della positività del linfonodo sentinella; altre strutture, invece, utilizzano una metodica di diagnostica intra-operatoria che nonostante il buon grado di sensibilità, può generare dei falsi negativi. Solo una minima parte delle strutture in Regione è dotata, infatti, di uno strumento ad alta sensibilità come la One Step Nucleic acid Amplification (OSNA) con elevata accuratezza diagnostica. Sempre per ciò che concerne la parte chirurgica, il KPI 4 ha mostrato il valore del 4% di re-interventi, in linea con i dati di lettura internazionale. Andando ad analizzare i valori inerenti all’area della terapia adiuvante, il KPI 5 ha evidenziato un’inappropriatezze da under-use (solo il 71% delle pazienti inizia la terapia adiuvante entro 60 giorni dalla data dell’ultimo intervento). Questo tipo di trattamento ha una forte correlazione con gli outcome e gli esiti di salute essendo l’efficacia della terapia adiuvante tempo dipendente. La radioterapia (KPI 6) dimostra alcune criticità andando a mettere in luce un’area di under-use soprattutto per le pazienti non trattate con terapia adiuvante: il 70% inizia la terapia entro 150 giorni dall’intervento, mentre il 94% delle donne trattate con terapia adiuvante inizia la radioterapia entro 270 giorni. Questo risultato potrebbe essere correlato a criticità organizzative del percorso di cura. Andando, invece, a valutare la fase di follow-up, il KPI 7 presenta una delle maggiori criticità legata all’over-use della diagnostica post intervento. Come si evince dai risultati, il 72% delle pazienti nei dodici mesi consecutivi l’intervento (esclusi i primi due mesi analizzati nel KPI 2) sono sottoposte a diagnostiche non indicate dalle linee guida; tale valore è da ricondurre alle cause già discusse ed analizzate nel KPI 2.
Conclusioni
Lo studio, evidenziando nel complesso dei buoni livelli di qualità delle cure, ha messo in luce una serie di inappropriatezze nel percorso delle pazienti affette da carcinoma della mammella andando a sottolineare il concetto di come sia opportuno lavorare per rendere i clinici e i decisori più attenti ad efficacia ed efficienza. Analizzando i risultati è emersa l’opportunità di pianificare delle discussioni strutturate con i clinici, al fine di giungere ad indicazioni condivise in alcuni ambiti del percorso di cura là dove siano ancora poco definite le indicazioni di letteratura. È inoltre emerso come “fare appropriatezza” non significhi unicamente risparmiare, in quanto tale situazione è abitualmente associata all’area dell’over-use; è infatti importante porre altrettanta attenzione anche all’area dell’under-use (concentrandosi quindi su pazienti che per il loro reale bisogno di salute dovrebbero ricevere un trattamento, ma che il sistema non eroga), come evidenziato in figura 1.
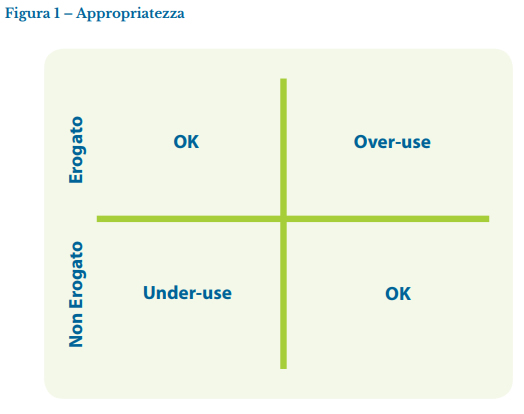
Diventa pertanto strategico, al fine di garantire la sostenibilità del sistema sanitario, riallocare le risorse risparmiate facendo appropriatezza nell’area dell’over-use verso l’area dell’under-use, passando così concretamente da costi evitabili a costi evitati.
Il progetto ha, infine, dimostrato come sia possibile monitorare alcuni indicatori di processo mediante l’utilizzo di flussi informativi correnti al fine di ottenere una migliore Governance del sistema.
Alla luce di quanto è emerso dal progetto, in futuro sarebbe auspicabile ed opportuno cercare di transitare dal sistema di remunerazione a prestazione (sistema DRG, Nomenclatore Tariffario per prestazioni ambulatoriali) verso un sistema di rimborsi correlati ai profili di cura, aggiornati per il reale assorbimento di risorse.
Bibliografia
1. 2° Rapporto GIMBE sulla sostenibilità del SSN – presentato a Roma il 6 giugno 2017
2. Il Governo Clinico nelle Aziende Sanitarie Versione 1.4 del 6 febbraio 2009 – GIMBE
3. The challenge of sustainability in healthcare systems: Frequency and cost of inappropriate
patterns of breast cancer care (the E.Pic.A study) – Massa et al.,
4. The Breast 34 (2017) 103-107
5. Programma Nazionale Esiti
http://95.110.213.190/PNEedizione16_p/index.php?lang=IT
6. Linee guida: neoplasie della mammella (breast cancer guidelines) (updated to October
19th 2016) Associazione Italiana di Oncologia Medica (AIOM)
([Accessed 26 January 2017])
http://www.aiom.it/professionisti/documenti-scientifici/linee
guida/1%2C413%2C1%2C
7. L’equilibrio tra appropriatezza prescrittiva e sostenibilità economica: dagli indicatori
di consumo agli indicatori di percorso Balancing prescription appropriateness and
economic sustainability: from consumption indicators to pathway indicators – Luca
Degli Esposti, Giornale Italiano di Farmacoeconomia e Farmacoutilizzazione 2014